Pixabay
Todos los médicos aspiramos a tener poderes milagrosos para aliviar el sufrimiento. Hay oportunidades, por ejemplo cuando uno atiende a un niño de 3 años con codo de niñera. Un poco de supinación y flexión (o si uno es más moderno quizás la hiperpronación) y el alivio es total e instantánea. El asombro y felicidad de la madre cuando se da cuenta que su hijo ya no tiene nada de dolor es total. Uno queda contento que su paciente está bien y como si fuera poco ¡Además la familia está agradecida!
Lastimosamente no hay tratamientos parecidos en terminos de lo milagroso para muchas enfermedades en la medicina interna. Hoy vamos a hablar de un medicamento que algunos médicos utilizan mucho para aproximarse a los milagros: la familia de esteroides que se llama glucocorticoides. Sería fácil escribir múltiples volúmenes sobre este tema, pero vamos a sintetizar lo más esencial que uno necesita saber.
Lastimosamente no hay tratamientos parecidos en terminos de lo milagroso para muchas enfermedades en la medicina interna. Hoy vamos a hablar de un medicamento que algunos médicos utilizan mucho para aproximarse a los milagros: la familia de esteroides que se llama glucocorticoides. Sería fácil escribir múltiples volúmenes sobre este tema, pero vamos a sintetizar lo más esencial que uno necesita saber.
¿Qué son los glucocorticoides?
El cortisol es un esteroide endógena natural que se produce en la zona fascicular de las glándulas suprarrenales y produce múltiples efectos sobre el organismo, principalmente en cuanto a disminuir la respuesta inflamatoria, desactivar el sistema inmunológico, aumentar la presión arterial, aumentar la glucosa de la sangre, aumentar la obesidad central, aumentar el leucocitosis, y disminuir la densidad ósea.
http://www.ncbi.nlm.nih.gov/books/NBK13780/
El cortisol es un esteroide endógena natural que se produce en la zona fascicular de las glándulas suprarrenales y produce múltiples efectos sobre el organismo, principalmente en cuanto a disminuir la respuesta inflamatoria, desactivar el sistema inmunológico, aumentar la presión arterial, aumentar la glucosa de la sangre, aumentar la obesidad central, aumentar el leucocitosis, y disminuir la densidad ósea.
http://www.ncbi.nlm.nih.gov/books/NBK13780/
¿Cómo es que los glucocorticoides disminuyen la respuesta inflamatoria y las defensas contra infección?
El primer paso es que glucocorticoide se une al receptor GR en el citosol de las células. El complejo activado GR se traslada al núcleo celular donde se une al receptor GRE (elementos de respuesta glucocorticoide) que es un regulador de expresión genética resultando en la expresión de las proteínas antiinflamatorias (lipocortin I, SLPI, MAPK fosfatasa) y aumenta la expresión de proteínas anti-inflamatorias en un proceso que se llama transactivación. También reprime la expresión de las proteínas pro-inflamatorias. Esto se llama transrepresión.
Los glucocorticoides activan lipocortinas que inhiben fosfolipasa A2, una enzima que actua sobre los fosfolípidos de la membrana plasmática para liberar ácido araquidónico. Este es un paso antes del paso donde actúan los AINES y resulta en disminuido síntesis de numerosos prostanoides y leucotrienos, incluyendo PGE y leucotrieno B4. Leucotrieno B4 es generado por los neutrófilos y macrofágos como respuesta a estimulación y es un factor esencial para la adhesión, quimiotaxis y agregación de leucocitos para combatir infección. Prostaglandina E causa vasodilatación y promueve la migración de neutrófilos, macrófagos y mastocitos al sitio de infección.
Los glucocorticoides resultan en la desmarginación de los neutrófilos, resultando en neutrofilia y leucocitosis, pero al mismo tiempo estabiliza las membranas de los lisosomas y gránulos secretorios y causa inhibición de exocitosis para que no pueden soltar los leucotrienos. O sea que esencialmente hay neutrofilia, pero los neutrófilas están incapacitados para actuar.
Es importante entender que debido al efecto de los glucocorticoides sobre Leucotrieno B4 y PGE cualquier síntoma de infección no va a manifestar hasta que el esteroide haya desaparecido del sistema del paciente. Puede haber infección extensa y diseminada, pero su presencia es indetectable debido a la ausencia de eritema, fiebre o dolor.
El primer paso es que glucocorticoide se une al receptor GR en el citosol de las células. El complejo activado GR se traslada al núcleo celular donde se une al receptor GRE (elementos de respuesta glucocorticoide) que es un regulador de expresión genética resultando en la expresión de las proteínas antiinflamatorias (lipocortin I, SLPI, MAPK fosfatasa) y aumenta la expresión de proteínas anti-inflamatorias en un proceso que se llama transactivación. También reprime la expresión de las proteínas pro-inflamatorias. Esto se llama transrepresión.
Los glucocorticoides activan lipocortinas que inhiben fosfolipasa A2, una enzima que actua sobre los fosfolípidos de la membrana plasmática para liberar ácido araquidónico. Este es un paso antes del paso donde actúan los AINES y resulta en disminuido síntesis de numerosos prostanoides y leucotrienos, incluyendo PGE y leucotrieno B4. Leucotrieno B4 es generado por los neutrófilos y macrofágos como respuesta a estimulación y es un factor esencial para la adhesión, quimiotaxis y agregación de leucocitos para combatir infección. Prostaglandina E causa vasodilatación y promueve la migración de neutrófilos, macrófagos y mastocitos al sitio de infección.
Los glucocorticoides resultan en la desmarginación de los neutrófilos, resultando en neutrofilia y leucocitosis, pero al mismo tiempo estabiliza las membranas de los lisosomas y gránulos secretorios y causa inhibición de exocitosis para que no pueden soltar los leucotrienos. O sea que esencialmente hay neutrofilia, pero los neutrófilas están incapacitados para actuar.
Es importante entender que debido al efecto de los glucocorticoides sobre Leucotrieno B4 y PGE cualquier síntoma de infección no va a manifestar hasta que el esteroide haya desaparecido del sistema del paciente. Puede haber infección extensa y diseminada, pero su presencia es indetectable debido a la ausencia de eritema, fiebre o dolor.
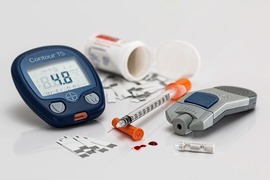
| ¿Cómo es que los glucocorticoides aumentan el nivel de la glucosa? Hay varios mecanismos de como los glucocorticoides aumentan la glucosa (de aquí el nombre) y desenmascaran la diabetes tipo II .
Para leer más sobre glucocorticoides y diabetes: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC4112077/ |
Pixabay
¿Cómo es que los glucocorticoides aumentan la presión arterial?
El efecto de los glucocorticoides para producir hipertensión es indisputable, sin embargo como es multifactorial varios investigadores ponen más peso sobre un mecanismo u otro mecanismo.
http://www.medscape.com/viewarticle/582385_4
El efecto de los glucocorticoides para producir hipertensión es indisputable, sin embargo como es multifactorial varios investigadores ponen más peso sobre un mecanismo u otro mecanismo.
- Los glucocorticoides aumentan la expresión de angiotensinógeno (el precursor de la angiotensina I) en los hepatocitos.
- Renina secretado por el aparato yuxtaglomerular de los riñones actúa sobre la angiotensinógeno para producir Angiotensina I
- Glucocorticoides aumentan la expresión de la enzima ECA, presente en el endotelio vascular de los pulmones y las células epiteliales de los riñones. ECA convierte angiotensina I a II.
- Glucocorticoides aumentan la expresión del receptor Angiotensina II tipo I
- Angiotensina II une con el receptor de Angiotensina II y modula la vasoconstricción y la secreción de aldosterona. La vasoconstricción sube la presión arterial
- Angiotensina II también actúa sobre la glándula pituitaria posterior para estimular la secreción de ADH (La hormona anti-diurética) con efectos de vasoconstricción y actúa para aumentar la permeabilidad y la reabsorción de agua en el conducto colector que resulta en edema.
- La aldosterona aumenta el transporte de sodio en el nefrón distal y la expansión de volumen. (Aunque este efecto es más pronunciado con los mineralocorticoides como fludricortisona.)
http://www.medscape.com/viewarticle/582385_4
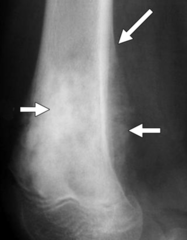
| ¿Cómo es que los glucocorticoides causan osteoporosis? Glucorticoides estimulan la resorción ósea (osteoclastogénesis). En los primeros meses de tratamiento la densidad mineral ósea disminuye 10%, con más perdida del hueso trabecular que el hueso cortical. Esto predispone a fracturas, principal entre ellos las fracturas vertebrales aunque también puede haber fracturas de la cadera. Para leer más sobre glucocorticoides y osteoporosis: http://www.ncbi.nlm.nih.gov/pubmed/12114261 http://www.ncbi.nlm.nih.gov/pubmed/17566815 http://www.medscape.com/viewarticle/775072_2 http://www.ncbi.nlm.nih.gov/pubmed/1211426 |
¿Hay diferencias entre los glucocorticoides?
¡Claro que si!
¡Claro que si!
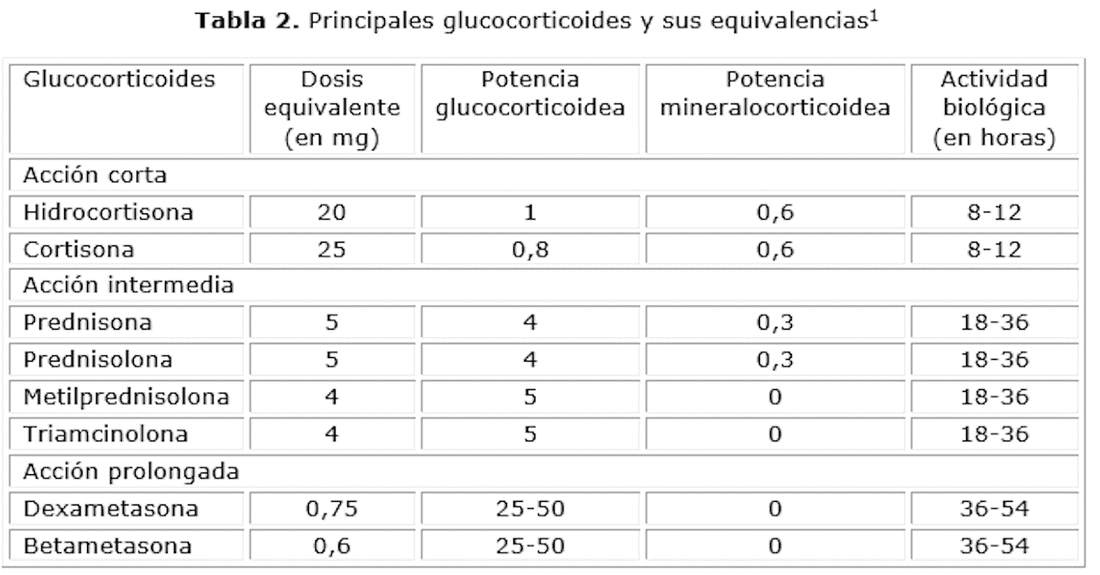
- Hay distintas potencias de corticoesteroides. La hidrocortisona (cortisol) es de acción corta y es la forma natural. Los otros glucocorticoides son sintéticos y más potentes.
- Nota la duración de actividad biológica. Dosis repetidas de glucocorticoides como beclometasona o dexametasona a nivel diario pueden acumular en el sistema del paciente y suprimir más seriamente el sistema inmunológico.
- Nota que los glucocorticoides con mayor potencia mineralocorticoidea causan más hipertensión.
¿Hay circunstancias donde es apropiado utilizar glucocorticoides?
Enfermedades que son caracterizados por hiperactividad de la respuesta inflamatoria pueden beneficiar del uso de glucocorticoides. El eje central de la dosificación de glucocorticoides es utilizar la potencia más baja en el dosis más bajo por la duración más breve que logra el objetivo que uno está buscando.
http://ard.bmj.com/content/early/2016/03/01/annrheumdis-2015-208916.abstract
Asma
Es de recordar que la base del tratamiento de asma es la eliminación del medio ambiente de los fómites que desatan la respuesta inflamatoria, por ejemplo la eliminación de cobijas y animales de peluche, colchones y almohadas viejas, y sofás y alfombras que pueden servir como criaderos de ácaro de polvo.
Hay tratamientos más modernos para controlar asma que tienen menos efectos adversos. Uno de los principales es montelukast, con o sin loratidina, para controlar la rinitis alérgica crónica que provoca el goteo posnasal que precipita la exacerbación de las síntomas de asma. Montelukast también es de utilidad para controlar el asma inducido por ejercicio.
El papel de los esteroides es como una intervención oportuna y breve para contener una exacerbación. En una exacerbación leve se podría considerar un esteroide como beclometasona o triamcinolona inhalada diariamente por unas semanas. En una exacerbación más serio entonces un pulso de tres a cinco días de prednisona o prednisolona por vía oral. Normalmente no se utiliza glucocorticoides potentes como dexametasona o betametasona por vía oral o endovenoso al menos que uno va a dar dosis única para una obstrucción de la vía aérea, por ejemplo en crup o anafilaxia.
Enfermedades que son caracterizados por hiperactividad de la respuesta inflamatoria pueden beneficiar del uso de glucocorticoides. El eje central de la dosificación de glucocorticoides es utilizar la potencia más baja en el dosis más bajo por la duración más breve que logra el objetivo que uno está buscando.
http://ard.bmj.com/content/early/2016/03/01/annrheumdis-2015-208916.abstract
Asma
Es de recordar que la base del tratamiento de asma es la eliminación del medio ambiente de los fómites que desatan la respuesta inflamatoria, por ejemplo la eliminación de cobijas y animales de peluche, colchones y almohadas viejas, y sofás y alfombras que pueden servir como criaderos de ácaro de polvo.
Hay tratamientos más modernos para controlar asma que tienen menos efectos adversos. Uno de los principales es montelukast, con o sin loratidina, para controlar la rinitis alérgica crónica que provoca el goteo posnasal que precipita la exacerbación de las síntomas de asma. Montelukast también es de utilidad para controlar el asma inducido por ejercicio.
El papel de los esteroides es como una intervención oportuna y breve para contener una exacerbación. En una exacerbación leve se podría considerar un esteroide como beclometasona o triamcinolona inhalada diariamente por unas semanas. En una exacerbación más serio entonces un pulso de tres a cinco días de prednisona o prednisolona por vía oral. Normalmente no se utiliza glucocorticoides potentes como dexametasona o betametasona por vía oral o endovenoso al menos que uno va a dar dosis única para una obstrucción de la vía aérea, por ejemplo en crup o anafilaxia.
¿Hay situaciones donde se debe utilizar glucocorticoides todos los días?
Hay algunas enfermedades autoinmunes donde es imprescindible utilizar glucocorticoides de potencia y dosis muy bajo todos los días. Un ejemplo común es lupus eritematosos sistémico donde la utilización de dosis bajo de prednisona o prednisolona es necesario para evitar el desarrollo de insuficiencia renal. Otros ejemplos de enfermedades donde en algunos casos se utilizan glucocorticoides todos los días en dosis muy bajo son el la enfermedad de Crohns, colitis ulcerativa, y para evitar el rechazo a los trasplantes de órganos.
Hay situaciones como la enfermedad de Addison y la hiperplasia suprarrenal congénita donde iniciamos tratamiento con un dosis elevado de hidrocortisona para estabilizar al paciente y se transiciona a un dosis bajo de un mineralocorticoide como fludricortisona para el uso diario precisamente con el objetivo de subir la presión y la glucosa.
Cuando una persona tiene una historia de uso crónica de glucocorticoides hay una practica de la década de los 50 que las glándulas suprarrenales están suprimidas y hay que suplementar con dosis suprafisiológicas antes de la cirugía. Actualmente la evidencia científica no respalda esta practica, sin embargo es de considerar suplementar con esteroides si hay hipotensión inexplicable perioperatoria en pacientes que normalmente usan glucocorticoides todos los días.
Hay enfermedades donde el uso de glucocorticoides es muy controvertido, principal entre ellos el EPOC y el artritis reumatoide. En el caso de EPOC se ha cambiado de uso crónico al uso solamente cuando hay exacerbaciones. Si Ud maneja pacientes con EPOC o artritis reumatoide es importante actualizarse y tomar en cuenta si su paciente padece de diabetes, hipertensión o osteoporosis o obesidad, ya que los esteroides van a empeorar la glucosa, la presión y la resistencia a infecciones.
Para leer más:
http://www.ncbi.nlm.nih.gov/pubmed/27256352
http://www.ncbi.nlm.nih.gov/pubmed/23695200
Hay algunas enfermedades autoinmunes donde es imprescindible utilizar glucocorticoides de potencia y dosis muy bajo todos los días. Un ejemplo común es lupus eritematosos sistémico donde la utilización de dosis bajo de prednisona o prednisolona es necesario para evitar el desarrollo de insuficiencia renal. Otros ejemplos de enfermedades donde en algunos casos se utilizan glucocorticoides todos los días en dosis muy bajo son el la enfermedad de Crohns, colitis ulcerativa, y para evitar el rechazo a los trasplantes de órganos.
Hay situaciones como la enfermedad de Addison y la hiperplasia suprarrenal congénita donde iniciamos tratamiento con un dosis elevado de hidrocortisona para estabilizar al paciente y se transiciona a un dosis bajo de un mineralocorticoide como fludricortisona para el uso diario precisamente con el objetivo de subir la presión y la glucosa.
Cuando una persona tiene una historia de uso crónica de glucocorticoides hay una practica de la década de los 50 que las glándulas suprarrenales están suprimidas y hay que suplementar con dosis suprafisiológicas antes de la cirugía. Actualmente la evidencia científica no respalda esta practica, sin embargo es de considerar suplementar con esteroides si hay hipotensión inexplicable perioperatoria en pacientes que normalmente usan glucocorticoides todos los días.
Hay enfermedades donde el uso de glucocorticoides es muy controvertido, principal entre ellos el EPOC y el artritis reumatoide. En el caso de EPOC se ha cambiado de uso crónico al uso solamente cuando hay exacerbaciones. Si Ud maneja pacientes con EPOC o artritis reumatoide es importante actualizarse y tomar en cuenta si su paciente padece de diabetes, hipertensión o osteoporosis o obesidad, ya que los esteroides van a empeorar la glucosa, la presión y la resistencia a infecciones.
Para leer más:
http://www.ncbi.nlm.nih.gov/pubmed/27256352
http://www.ncbi.nlm.nih.gov/pubmed/23695200
¿Se puede utilizar glucocorticoides en casos de infección?
Normalmente es una malísima idea utilizar glucocorticoides en situaciones de infección ya que el medicamento encubre las síntomas y deshabilita las defensas contra infección y permite que la infección se extiende silenciosamente, especialmente en el caso de tuberculosis, infecciones por Candida, y todo tipo de infección en los diabeticos.
Normalmente es una malísima idea utilizar glucocorticoides en situaciones de infección ya que el medicamento encubre las síntomas y deshabilita las defensas contra infección y permite que la infección se extiende silenciosamente, especialmente en el caso de tuberculosis, infecciones por Candida, y todo tipo de infección en los diabeticos.
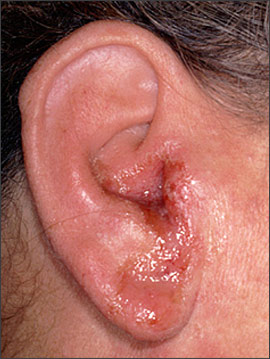
| .El paciente que recibe dosis de esteroides de alta potencia puede tener una infección y al mismo permanecer asintomático hasta 3 a 9 días después de suspender el glucocorticoide, cuando de repente aparece las evidencias de infección como eritema, dolor, temperatura etc. A veces la infección que florece es trivial, por ejemplo Candida oral o vaginal, pero en otros casos puede ser más grave por ejemplo Tuberculosis fulminante o un pie diabético infectado. Un ejemplo es cuando glucocorticoides precipitan descompensación de la glucosa en individuos que ya tenían principios de Diabetes tipo II pero eran asintomáticos. Otitis externa maligna por Pseudomonas es en muchos casos la primera infección que anuncia la presencia de diabetes, y no es raro que la otitis externa maligna se manifiesta por primera vez 5 días después de descontinuar los glucocorticoides. |
Sin embargo cabe mencionar que hay excepciones donde si se utiliza glucocorticoides en la presencia de infección. El principal entre ellos es la meningitis provocado por la bacteria Haemophilus influenza. La administración de dosis única de un glucocorticoide el primer día antes de iniciar tratamiento con antibioticos puede proteger la audición del paciente. Igual ocurre en el crup, una infección viral donde se da dosis única de dexametasona.
Uno de los grandes consecuencias del uso de los glucocorticoides ocurre si se administra accidentalmente en un paciente con herpes zóster oftálmico, ya que esto puede provocar ceguera. Por esto el uso de colirios oftálmicos de antibióticos mezclado con glucocorticoides es muy arriesgado. En general el recetar colirios con glucocorticoides debe ser campo exclusivo del oftalmólogo ya que queda bajo su responsibilidad realizar una prueba de fluoresceina para garantizar que su paciente no tiene lesiones dendriticas en la cornea antes de administrar colirios con esteroides.
Actualmente el uso de glucocorticoides para elevar la presión en cuidados intensivos en casos de choque séptico recalcitrante es muy controvertido en cuanto a las evidencias y trasciende este articulo.
Para leer más sobre el uso de glucocorticoides en meningitis por Haemophilus influenzae
http://www.cochrane.org/CD004405/ARI_corticosteroids-bacterial-meningitis
Uno de los grandes consecuencias del uso de los glucocorticoides ocurre si se administra accidentalmente en un paciente con herpes zóster oftálmico, ya que esto puede provocar ceguera. Por esto el uso de colirios oftálmicos de antibióticos mezclado con glucocorticoides es muy arriesgado. En general el recetar colirios con glucocorticoides debe ser campo exclusivo del oftalmólogo ya que queda bajo su responsibilidad realizar una prueba de fluoresceina para garantizar que su paciente no tiene lesiones dendriticas en la cornea antes de administrar colirios con esteroides.
Actualmente el uso de glucocorticoides para elevar la presión en cuidados intensivos en casos de choque séptico recalcitrante es muy controvertido en cuanto a las evidencias y trasciende este articulo.
Para leer más sobre el uso de glucocorticoides en meningitis por Haemophilus influenzae
http://www.cochrane.org/CD004405/ARI_corticosteroids-bacterial-meningitis
Evitar el síndrome de deprivación glucocorticoidea
Debido a los efectos adversos de glucocorticoides es inevitable que donde se puede descontinuar lo vamos a hacer lo más pronto posible. Si su paciente ha utilizado glucocorticoides por más que 8 días se reduce la dosis gradualmente sobre 3 a 4 semanas para no precipitar el síndrome de deprivación glucocorticoidea. Hay varios regímenes que se puede utilizar (por ejemplo dos pastillas al día por una semana, una pastilla al día por una semana, media pastilla al dia por una semana, media pastilla un día sí un día no por una semana). Lo esencial es que igual como es el caso con los beta-bloqueadores, las benzodiazepinas y los narcóticos opiatos, el uso crónico crea una adicción, y la abstinencia repentina es muy peligrosa y causa sufrimiento considerable para su paciente.
Por supuesto mantenga en mente que hay enfermedades donde nunca se descontinua glucocorticoides por ejemplo lupus eritematosa sistémica, hiperplasia adrenal congénita, y trasplante de órganos.
Para leer más sobre descontinuación de glucocorticoides puede leer aquí:
http://onlinelibrary.wiley.com/doi/10.1002/psb.1060/pdf
Debido a los efectos adversos de glucocorticoides es inevitable que donde se puede descontinuar lo vamos a hacer lo más pronto posible. Si su paciente ha utilizado glucocorticoides por más que 8 días se reduce la dosis gradualmente sobre 3 a 4 semanas para no precipitar el síndrome de deprivación glucocorticoidea. Hay varios regímenes que se puede utilizar (por ejemplo dos pastillas al día por una semana, una pastilla al día por una semana, media pastilla al dia por una semana, media pastilla un día sí un día no por una semana). Lo esencial es que igual como es el caso con los beta-bloqueadores, las benzodiazepinas y los narcóticos opiatos, el uso crónico crea una adicción, y la abstinencia repentina es muy peligrosa y causa sufrimiento considerable para su paciente.
Por supuesto mantenga en mente que hay enfermedades donde nunca se descontinua glucocorticoides por ejemplo lupus eritematosa sistémica, hiperplasia adrenal congénita, y trasplante de órganos.
Para leer más sobre descontinuación de glucocorticoides puede leer aquí:
http://onlinelibrary.wiley.com/doi/10.1002/psb.1060/pdf
Uso empírico de glucocorticoides
El uso empírico de glucocorticoides sistémicos para síntomas de causa desconocida por ejemplo fiebre, dolor, infección, anormalidades de laboratorio, o tos es una forma de mala praxis que es condenable ya que uno está exponiendo el paciente a numerosos efectos adversos (hiperglicemia, hipertensión, infección, osteoporosis, obesidad, cataratas y síndromes de abstinencia) sin garantía alguna de beneficio para el paciente. El hecho de que las síntomas pueden no manifestarse hasta después que se descontinua el medicamento hace que el paciente no descubre y no atribuye la causa al medicamento.
El uso empírico de glucocorticoides sistémicos para síntomas de causa desconocida por ejemplo fiebre, dolor, infección, anormalidades de laboratorio, o tos es una forma de mala praxis que es condenable ya que uno está exponiendo el paciente a numerosos efectos adversos (hiperglicemia, hipertensión, infección, osteoporosis, obesidad, cataratas y síndromes de abstinencia) sin garantía alguna de beneficio para el paciente. El hecho de que las síntomas pueden no manifestarse hasta después que se descontinua el medicamento hace que el paciente no descubre y no atribuye la causa al medicamento.
| ¿Y si los glucocorticoides causan tantos efectos adversos porque tantos médicos los usan? Muy sencillo. El médico da corticoesteroides para la satisfacción del cliente, es decir para caerle bien. Como quita el dolor, la inflamación, y las sibilancias del paciente entre 6 a 12 horas, el paciente esta´satisfecho con el tratamiento “milagroso” y no va a ir a otro médico. El problema es que al menos que el paciente tenga un problema autoinmune esta sensación de bienestar no corresponde con la realidad. Mientras lo toma se siente bien y no se da cuenta que tiene la presión arterial y la glucosa alta. Sube de peso y puede desarrollar osteoporosis y cataratas. Al parar el medicamento vuelve las síntomas y más entre 3 y 5 días y el paciente vuelve al médico para otra receta, pero esta vez las recetas van a ser para esteroides, antibióticos para la infección iatrogénica, agentes antidiabéticos y antihipertensivos. O sea que el médico conscientamente o inconscientamente ha creado un cliente permanente para todas las enfermedades que el glucocorticoid ha precipitado y que van a manifestarse cada vez que el paciente trata de descontinuarlos. |






 Canal RSS
Canal RSS